La suplementación útil exige algo más que entusiasmo: requiere evidencia, contexto y criterio. Esta publicación revisa algunos de los suplementos con mejor respaldo científico y delimita con precisión en qué situaciones pueden aportar una ventaja real, para qué perfiles resultan más pertinentes y qué límites conviene tener presentes. A lo largo del texto se abordan ayudas ergogénicas como el bicarbonato, los nitratos, la creatina, la beta-alanina, el HMB y la proteína, atendiendo a su mecanismo de acción, dosis habituales, seguridad y aplicación práctica. El propósito es ofrecer una síntesis rigurosa y clara, útil para orientar decisiones y separar la utilidad real del ruido comercial. Pasen y lean.rucción
MAGNESIO
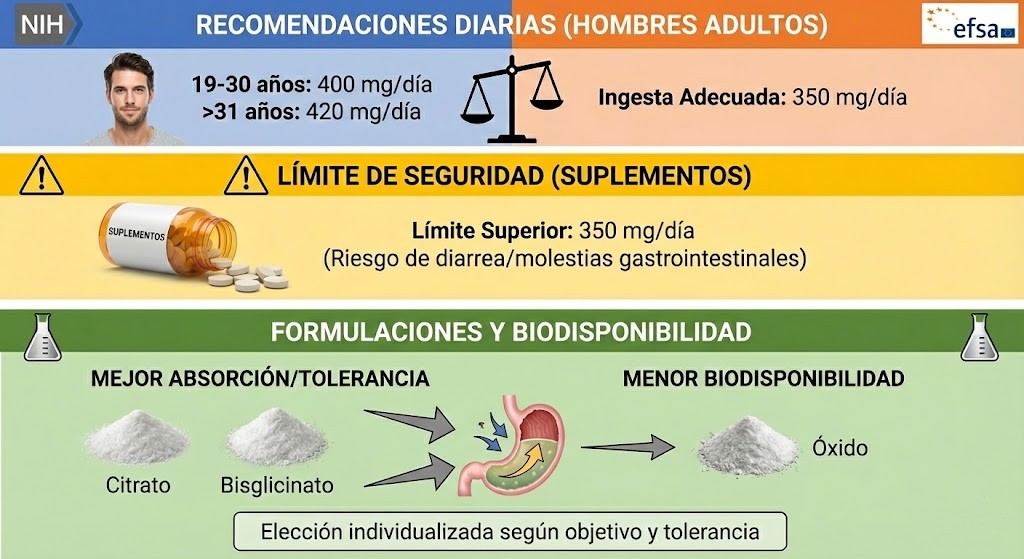
El magnesio actúa como un cofactor esencial en más de 600 reacciones enzimáticas, siendo vital para el metabolismo energético y la función neuromuscular. Cuando hablamos de adultos, la cifra “correcta” de magnesio no es única, porque depende del marco técnico que se adopte. En la hoja informativa del Office of Dietary Supplements (NIH), las ingestas recomendadas (RDA, por sus siglas en inglés, como en el resto de acrónimos que utilizaremos) se sitúan en 400 mg/día entre los 19 y los 30 años y en 420 mg/día desde los 31, mientras que la EFSA, al trabajar con una ingesta adecuada (AI), propone 350 mg/día para hombres adultos. La divergencia no nace de una discrepancia clínica directa, sino de metodologías distintas para estimar necesidades poblacionales y traducirlas a valores operativos en salud pública (EFSA NDA Panel, 2015; NIH ODS, 2026).
En el plano de la seguridad, el umbral práctico más citado es el límite superior tolerable (UL) para magnesio procedente de suplementos y medicamentos, fijado en 350 mg/día en adultos, ya que a partir de ahí aumenta la probabilidad de diarrea, náuseas o cólicos por el efecto osmótico de sales no absorbidas (Institute of Medicine, 1997; NIH ODS, 2026). Si bajamos al terreno de las formulaciones, conviene huir de la promesa de una “sal universal”: la literatura comparativa sugiere que formas como el citrato, y en ciertos contextos también quelatos tipo diglicinato, tienden a mostrar mejor biodisponibilidad o tolerancia que el óxido, pero el resultado final depende también de la dosis, la pauta, el estado gastrointestinal y la sensibilidad individual (Lindberg et al., 1990; Schuette et al., 1994; Walker et al., 2003). Por ello, la elección sensata debe individualizarse según objetivo clínico, tolerancia digestiva, interacciones farmacológicas y función renal (NIH ODS, 2026).
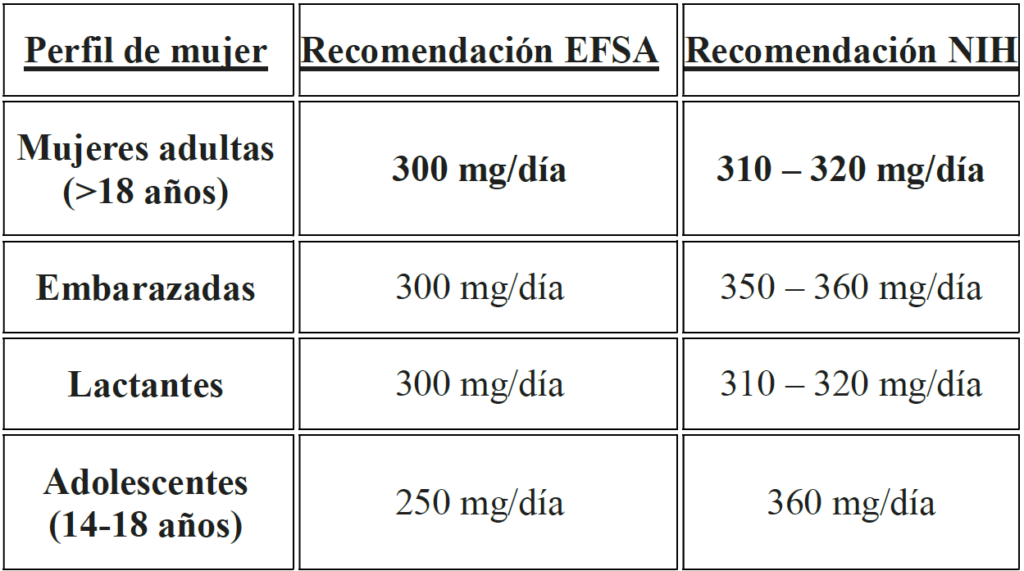
En el caso de mujeres adultas, la Autoridad Europea de Seguridad Alimentaria (EFSA, 2015) establece una AI de 300 mg/día procedentes de la dieta total. No obstante, en el ámbito de la suplementación, la EFSA determina un UL de 250 mg/día para las sales de magnesio (como el citrato o el bisglicinato), con el fin de prevenir efectos adversos gastrointestinales. En contraste, los Institutos Nacionales de Salud (NIH) de EE. UU. recomiendan una ingesta total de 310-320 mg/día, permitiendo hasta 350 mg/día en suplementos. La evidencia científica reciente (Sarić et al., 2025) destaca que mantener niveles séricos óptimos —preferiblemente por encima de 0.85 mmol/L— es fundamental durante la perimenopausia y la vejez para optimizar la salud ósea, la calidad del sueño y el rendimiento físico funcional.
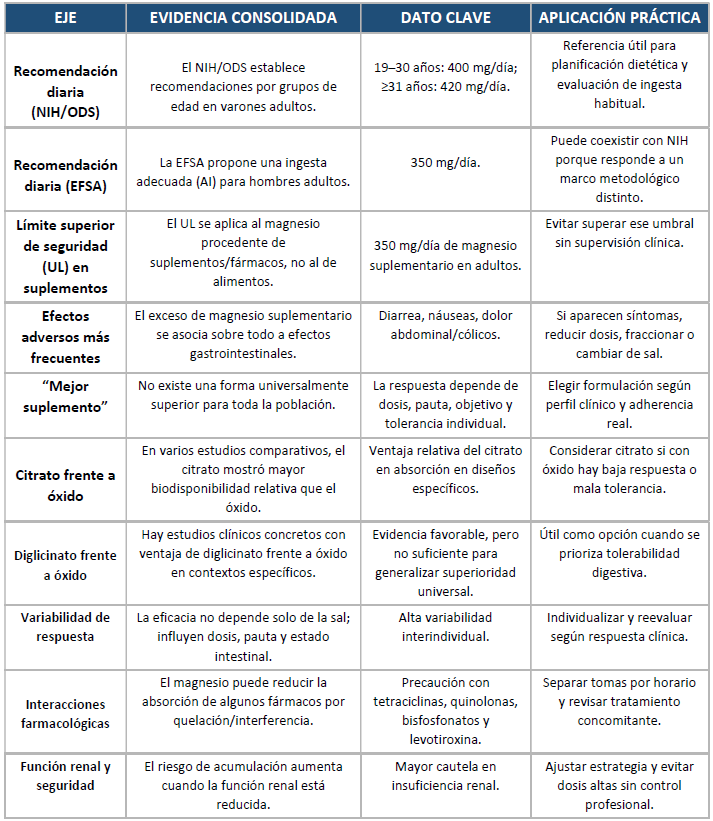
Nota. El UL de 350 mg/día corresponde al magnesio procedente de suplementos/fármacos; no incluye el magnesio ingerido en alimentos. Las cifras NIH y EFSA derivan de metodologías de referencia diferentes.
Bibliografía:
EFSA Panel on Dietetic Products, Nutrition and Allergies (NDA). (2015). Scientific opinion on dietary reference values for magnesium. EFSA Journal, 13(7), 4186.
EFSA Panel on Dietetic Products, Nutrition and Allergies. (2015). Scientific Opinion on Dietary Reference Values for magnesium. EFSA Journal, 13(7), 4164.
Institute of Medicine. (1997). Dietary reference intakes for calcium, phosphorus, magnesium, vitamin D, and fluoride. National Academies Press.
Lindberg, J. S., Zobitz, M. M., Poindexter, J. R., & Pak, C. Y. C. (1990). Magnesium bioavailability from magnesium citrate and magnesium oxide. Journal of the American College of Nutrition, 9(1), 48–55.
National Institutes of Health (NIH). (2022). Magnesium: Fact Sheet for Health Professionals. Office of Dietary Supplements.
National Institutes of Health, Office of Dietary Supplements. (2026). Magnesium: Fact sheet for health professionals.
Sarić, M. M., Sorić, T., Juko Kasap, Ž., et al. (2025). Magnesium: Health effects, deficiency burden, and future public health directions. Nutrients, 17(22), 3626.
Schuette, S. A., Lashner, B. A., & Janghorbani, M. (1994). Bioavailability of magnesium diglycinate vs magnesium oxide in patients with ileal resection. JPEN. Journal of Parenteral and Enteral Nutrition, 18(5), 430–435.
Walker, A. F., Marakis, G., Christie, S., & Byng, M. (2003). Mg citrate found more bioavailable than other Mg preparations in a randomised, double-blind study. Magnesium Research, 16(3), 183–191.
HMB
El β-hidroxi-β-metilbutirato (HMB), metabolito de la leucina, encaja mejor como herramienta de “conservación” que como promesa de crecimiento en metodologías de entrenamiento enfocado a la hipertrofia o de fuerza; su perfil más consistente es el de suplemento anticatabólico y de apoyo a la recuperación, especialmente cuando el músculo se enfrenta a estrés no acostumbrado o a periodos de pérdida por desuso. La nueva postura de la International Society of Sports Nutrition (ISSN), actualizada en 2025, lo consideran seguro y señalan que puede atenuar el daño muscular y favorecer la recuperación, pero matizan que, en atletas ya entrenados, los resultados sobre rendimiento y composición corporal son mixtos, de modo que su coste-beneficio como estrategia para “ganar tamaño” suele ser inferior al de ayudas con evidencia más estable (Wilson et al., 2013; Rathmacher et al., 2025). Donde la fisiología resulta especialmente ilustrativa es en la farmacodinámica aguda[1]: con Ca-HMB —la forma cálcica del HMB, es decir, unido al calcio—, una dosis única cercana a 3 g produce un pico plasmático rápido (en menos de 60 min; alrededor de 484 μM) y se acompaña de un aumento de síntesis proteica miofibrilar y una reducción de la degradación proteica, junto con señalización compatible con activación de mTORC1[2]; esto aporta plausibilidad mecanística, pero no equivale a prometer hipertrofia visible en cualquier contexto (Wilkinson et al., 2018).
Su “uso real”, en cambio, se vuelve nítido cuando dejamos de contemplarlo como una herramienta de crecimiento muscular y lo enfocamos a la estrategia donde muestra mayor utilidad: el no perder masa muscular. En adultos mayores sometidos a 10 días de reposo absoluto, el HMB preservó masa magra frente a placebo, grupo en el que se dieron pérdidas significativas en la masa muscular, un modelo clínicamente relevante de atrofia por inactividad (Deutz et al., 2013). En sarcopenia, una revisión sistemática y metaanálisis (Su et al., 2024) concluye beneficio en fuerza (con evidencia limitada para cambios consistentes en masa o rendimiento físico global), lo que desplaza el foco hacia la funcionalidad. Esto lo podemos sumar a los resultados de Cruz-Jentoft y colaboradores (2017), quienes encontraron hallazgos mediante los que podems afirmar que el HMB contrarresta específicamente los mecanismos de pérdida muscular relacionados con la edad. Aquí es donde el HMB muestra su utilidad con más nitidez: en escenarios de riesgo catabólico, inactividad o envejecimiento.
También aparecen hallazgos interesantes en cuanto a resistencia: en población sana, un metaanálisis informa que 3 g/día durante 2–12 semanas mejora de forma significativa el rendimiento en ejercicios de resistencia o endurance (como correr, ciclismo o natación) y el VO₂máx (SMD[3] aproximadas 0,38 y 0,25, respectivamente), aunque el mecanismo y la traslación a perfiles concretos deben interpretarse con prudencia (Fernández-Landa et al., 2024). En el plano hormonal, otro metaanálisis reciente encuentra aumento significativo[4] de testosterona circulante sin cambios significativos en cortisol, IGF-1 o GH —u hormona de crecimiento—. Esto sugiere un entorno fisiológico favorable, pero que no se traduce necesariamente en una hipertrofia visual inmediata o, tal como dicen los autores, «la magnitud de este cambio es pequeña y su relevancia fisiológica no está clara»[5] (Bideshki et al., 2025).
La literatura de posicionamiento de la International Society of Sports Nutrition (Wilson et al,. 2013) describe al HMB como un suplemento seguro y eficaz, capaz de atenuar el daño muscular inducido por el ejercicio y favorecer la recuperación en poblaciones entrenadas y no entrenadas. El documento sugiere mayor eficacia cuando se consume en proximidad al entrenamiento y, además, cuando se ha mantenido durante un periodo previo (se menciona 2 semanas antes de un esfuerzo). Pero donde cobra mayor relevancia, como mencionamos, es en situaciones de catabolismo o estrés no acostumbrado, lo que obliga a leer el suplemento en clave funcional más que estética.
Como veredicto, el HMB es un suplemento de vida media plasmática corta (aproximadamente 2–3 horas), con un perfil de seguridad favorable; su utilidad es más verosímil como apoyo para atenuar la pérdida musculoesquelética en contextos de desuso o catabolismo que como herramienta principal para obtener ganancias musculares en sujetos entrenados.

Bibliografía:
Bideshki, M. V., Sadeghi, O., Behzadi, M., Jozi, M., Eskandari Damaneh, H., & Rashidinejad, A. (2025). β-Hydroxy-β-methyl butyrate (HMB) supplementation elevates testosterone levels without significant changes to cortisol, IGF-1, or growth hormone in adults: A GRADE-assessed systematic review and meta-analysis. Frontiers in Nutrition, 12, 1582135.
Cruz-Jentoft, A. J. (2018). Beta-Hydroxy-Beta-Methyl Butyrate (HMB): From experimental data to clinical evidence in sarcopenia. Current Protein & Peptide Science, 19(7), 668–672.
Deutz, N. E. P., Pereira, S. L., Hays, N. P., Oliver, J. S., Edens, N. K., Evans, C. M., & Wolfe, R. R. (2013). Effect of β-hydroxy-β-methylbutyrate (HMB) on lean body mass during 10 days of bed rest in older adults. Clinical Nutrition, 32(5), 704–712.
Fernández-Landa, J., Todorovic, N., Santibañez-Gutierrez, A., Ostojic, S. M., Calleja-González, J., Sekulic, D., & Mielgo-Ayuso, J. (2024). Effects of HMB on endurance performance in a healthy population: A systematic review and meta-analysis. Journal of Strength and Conditioning Research, 38(4), e202–e210.
Rathmacher, J. A., Pitchford, L. M., Stout, J. R., Townsend, J. R., Jäger, R., Kreider, R. B., Campbell, B. I., … Antonio, J. (2025). International society of sports nutrition position stand: β-hydroxy-β-methylbutyrate (HMB). Journal of the International Society of Sports Nutrition, 22(1), 2434734.
Su, H., Zhou, H., Gong, Q., Xiang, Q., Shao, Y., Zhao, Y., Ling, H., Chen, X., Tong, Y., & Li, Y. (2024). The effects of β-hydroxy-β-methylbutyrate or HMB-rich nutritional supplements on sarcopenia patients: A systematic review and meta-analysis. Frontiers in Medicine, 11, 1348212.
Wilkinson, D. J., Hossain, T., Hill, D. S., Phillips, B. E., Crossland, H., Williams, J., … Smith, K. (2018). Impact of the calcium form of β-hydroxy-β-methylbutyrate upon human skeletal muscle protein metabolism. Clinical Nutrition, 37(6), 2068–2075.
Wilson, J. M., Fitschen, P. J., Campbell, B., et al. (2013). International Society of Sports Nutrition position stand: Beta-hydroxy-beta-methylbutyrate (HMB). Journal of the International Society of Sports Nutrition, 10(1), 6.
[1] Es decir, qué produce este suplemento en el organismo y, más en concreto, qué efectos biológicos provoca en el músculo tras ingerirlo. Al añadir «aguda», especifica que se trata del efecto a corto plazo, en horas, tras una dosis puntual, no de cambios tras semanas de uso. Si habláramos de su absorción y niveles en sangre y no de una dosis puntual, nos referiríamos a la farmacocinética.
[2] El mTORC1 es un complejo proteico celular que actúa como sensor de nutrientes y señal de crecimiento, activando procesos que aumentan la síntesis de proteínas en el músculo. Más adelante, hablaremos de esto por su relevancia en otros contextos.
[3] Esto quiere decir “diferencia de medias estandarizada” (standardized mean difference, siguiendo el acrónimo): una medida de tamaño del efecto que expresa la diferencia entre grupos en unidades de desviación estándar para poder comparar resultados entre estudios con escalas distintas.
[4] En ciencia, «significativo» es un término matemático que indica simplemente que el resultado no fue fruto de la casualidad, lo que no se traduce en un gran cambio, pudiendo ser este modesto.
[5] Lo que nos indica que, aunque el cambio existe, no se puede deducir que tal cambio produzca un efecto pragmático relevante o, dicho con otras palabras, si sirve para algo en la práctica.

CREATINA
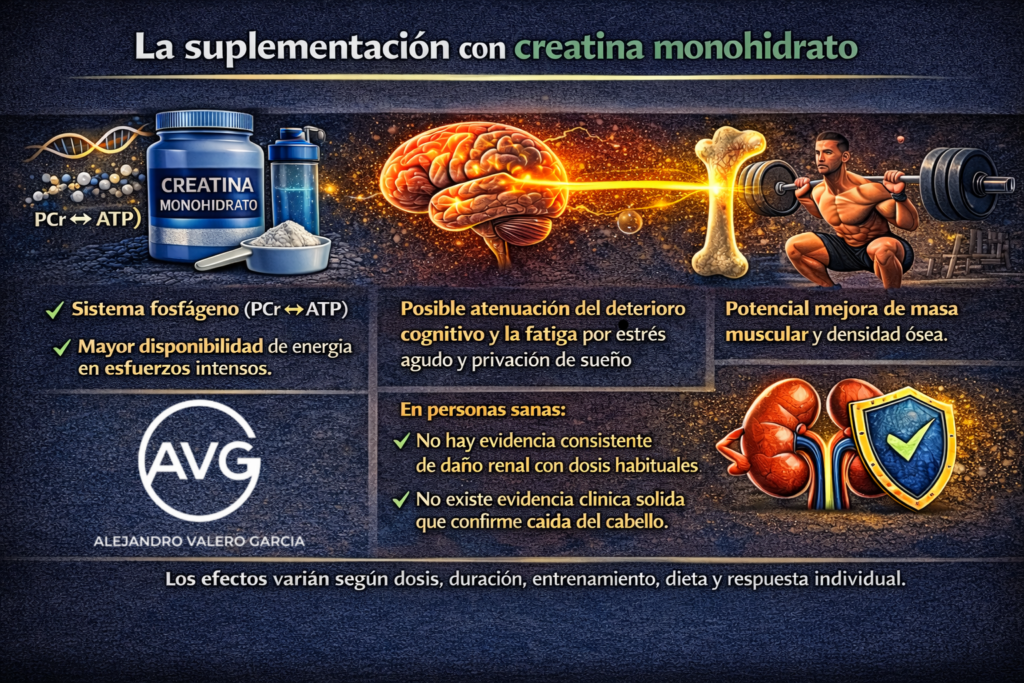
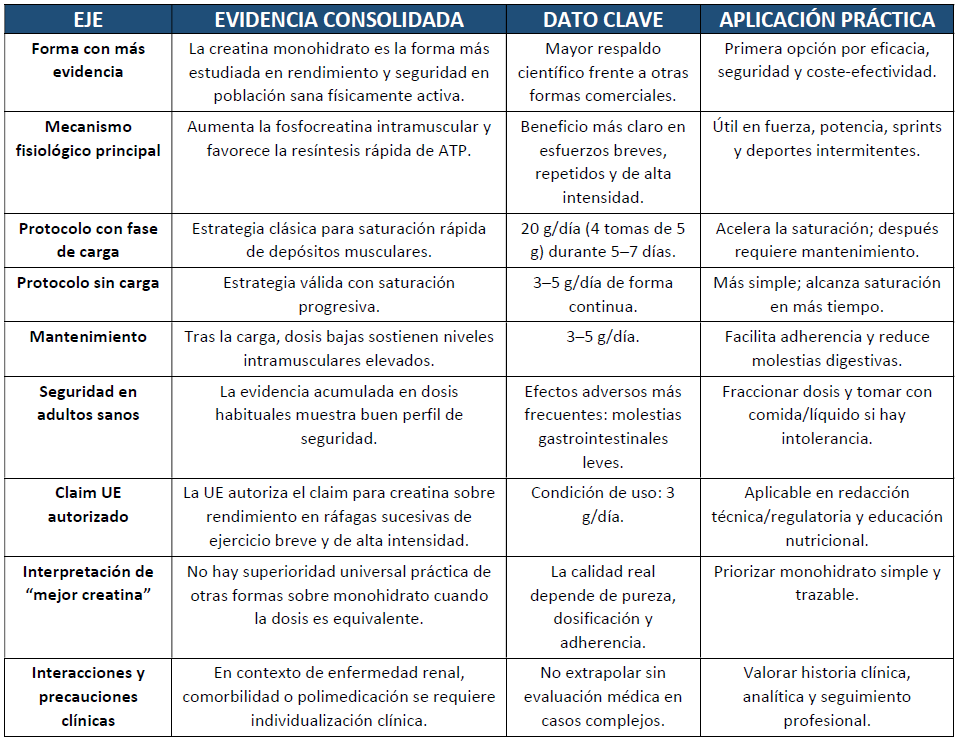
La creatina es un suplemento que incrementa las reservas musculares de fosfocreatina, una “reserva inmediata” de energía que ayuda a regenerar ATP con rapidez durante esfuerzos breves e intensos; así, permite sostener mejor la potencia y, a medio plazo, aprovechar más el entrenamiento y favorecer mejoras de fuerza y masa muscular principalmente. La creatina monohidrato sigue siendo la forma de referencia por volumen y consistencia de evidencia para rendimiento en esfuerzos breves, repetidos y de alta intensidad, y también para mejorar las adaptaciones al entrenamiento de fuerza[1]. Metaanálisis recientes muestran que, al combinarse con entrenamiento adecuado, la creatina aumenta la fuerza muscular en adultos y mejora variables de composición corporal (aumento de masa libre de grasa y reducción modesta de grasa corporal), aunque el tamaño del efecto varía según sexo, dosis, duración y características de la muestra (Desai et al., 2024; Wang et al., 2024; Ashtary-Larky et al., 2025).
La suplementación con creatina monohidrato (CrM, a partir de ahora) se reconoce actualmente como un modulador crítico del metabolismo energético celular a nivel sistémico, trascendiendo su uso tradicional en el rendimiento anaeróbico. Su función principal es la saturación de los depósitos de fosfocreatina, lo que permite mantener el ratio ATP[2]/ADP durante esfuerzos de alta intensidad y optimizar la resíntesis de glucógeno muscular (Kreider et al., 2017). Sin embargo, la vanguardia de la investigación destaca su papel en la salud cerebral; al actuar como una «lanzadera» (utilizan, concretamente, la palabra shuttle) de energía en neuronas y células gliales[3], la creatina ha demostrado mitigar el deterioro cognitivo inducido por el estrés agudo, la privación de sueño y posibles lesiones cerebrales traumáticas leves (Candow et al., 2023; Rawson et al., 2023). Investigaciones publicadas recientemente, como la de Mills y colaboradores (2024), han ampliado este espectro, demostrando que la suplementación de CrM combinada con entrenamiento de fuerza mejora significativamente la densidad mineral ósea en poblaciones adultas, combatiendo la osteosarcopenia.
En cuanto a la dosificación, los protocolos con mayor respaldo siguen siendo dos: una fase de carga de 20 g/día (habitualmente repartidos en 4 tomas de 5 g) durante 5–7 días, seguida de una fase de mantenimiento de 3–5 g/día, o bien una pauta continua de 3–5 g/día sin carga, que alcanza la saturación muscular de forma más lenta pero también eficaz (Kreider et al., 2017; NIH ODS, s. f.). Una revisión sistemática reciente añade un matiz práctico relevante: en adultos entrenados, el momento de la ingesta puede influir en la magnitud de la respuesta, con una tendencia favorable a la toma postentrenamiento. En ese contexto, una revisión sistemática reciente (Parada-Flores et al., 2025) describe como eficaces tanto una pauta relativa de 0,1 g/kg/día como una dosis fija de 5 g/día, siempre integradas en un programa de entrenamiento adecuado.
Más allá de los protocolos de carga, la evidencia insiste en un principio menos vistoso, pero más útil: la individualización. Se ha descrito que una pauta crónica de dosis bajas (3–5 g/día) puede bastar para alcanzar la saturación muscular en torno a las cuatro semanas, con la ventaja práctica de reducir la probabilidad de molestias gastrointestinales y de un aumento brusco de peso por retención hídrica (Antonio et al., 2021). En esa misma línea, una revisión sistemática con metaanálisis publicada en Nutrients (Wang et al., 2024) sugiere que, si el objetivo consiste en aumentar la fuerza muscular durante un protocolo de entrenamiento igual o superior a las cuatro semanas, la fase de carga no sería imprescindible, lo que refuerza el valor de estrategias más graduales y mejor toleradas.
Conviene subrayar que esta estrategia no debe interpretarse como una prerrogativa exclusiva de la suplementación, siendo preciso advertir que esta no es el único cauce para el rendimiento ni tampoco para un estado pleno de salud. Es imperativo realizar un llamamiento hacia una educación nutricional profunda, cuya meta final sea la suficiencia dietética; una en la que la necesidad de recurrir a ayudas exógenas sea la excepción y no la norma, interviniendo estas cuando el escenario biológico demande un refuerzo que el alimento, por sí solo, no alcance a cubrir.
A nivel regulatorio europeo, la alegación autorizada es precisa y no admite interpretaciones amplias: la creatina mejora el rendimiento físico en series sucesivas de ejercicio breve y de alta intensidad, siempre que se consuma una dosis de 3 g/día (EFSA NDA Panel, 2011; Comisión Europea, 2012). Por lo tanto, la conclusión técnicamente rigurosa no es que exista una “creatina universalmente superior” para cualquier persona y contexto, sino que el monohidrato sigue siendo la forma de referencia por solidez de evidencia, y que su uso debe ajustarse al objetivo, la dosis eficaz y la situación clínica individual (Ashtary-Larky et al., 2025; NIH ODS, s. f.).
Por último, conviene desmontar algunos mitos recurrentes a la luz de la evidencia disponible. Los consensos actuales reafirman que no existe evidencia científica que vincule este suplemento con el daño renal en individuos sanos o con la caída del cabello, manteniendo al monohidrato como la forma química de referencia por su estabilidad, su biodisponibilidad y la solidez del respaldo experimental acumulado (Antonio et al., 2021; Forbes et al., 2023).
Bibliografía:
Antonio, J., Candow, D. G., Forbes, S. C., Gualano, B., Jagim, A. R., Kreider, R. B., Rawson, E. S., Smith-Ryan, A. E., Castell, L. M., Hoffman, J. R., & VanDusseldorp, T. A. (2021). Common questions and misconceptions about creatine supplementation: What does the scientific evidence really show? Journal of the International Society of Sports Nutrition, 18(1), 13.
Ashtary-Larky, D., et al. (2025). Creatine supplementation and resistance training: A comparison between novice and experienced lifters—A systematic review and dose-response meta-analysis. Journal of the International Society of Sports Nutrition, 22(Suppl 1), Article 2586523.
Comisión Europea. (2012). Reglamento (UE) n.º 432/2012 de la Comisión, de 16 de mayo de 2012, por el que se establece una lista de declaraciones autorizadas de propiedades saludables en los alimentos. Diario Oficial de la Unión Europea, L136, 1–40.
Desai, I., Wewege, M. A., Jones, M. D., Clifford, B. K., Pandit, A., Kaakoush, N. O., Simar, D., & Hagstrom, A. D. (2024). The effect of creatine supplementation on resistance training–based changes to body composition: A systematic review and meta-analysis. Journal of Strength and Conditioning Research, 38(10), 1813–1821.
EFSA Panel on Dietetic Products, Nutrition and Allergies (NDA). (2011). Scientific opinion on the substantiation of health claims related to creatine and increase in physical performance during short-term, high intensity, repeated exercise bouts (ID 575, 1503, 1505, 1951) pursuant to Article 13(1) of Regulation (EC) No 1924/2006. EFSA Journal, 9(7), 2303.
European Commission. (n.d.). EU Register of nutrition and health claims made on foods (Creatine claim: improves physical performance in successive bursts of short-term, high intensity exercise; condition of use: 3 g/day).
Forbes, S. C., Cordingley, D. M., Cornish, S. M., Gualano, B., Roschel, H., Ostojic, S. M., Rawson, E. S., & Candow, D. G. (2023). Effects of Creatine Supplementation on Brain Health and Function in Healthy Individuals: A Systematic Review and Meta-Analysis. Sports Medicine, 53(Suppl 1), 67-85.
Kreider, R. B., Kalman, D. S., Antonio, J., Ziegenfuss, T. N., Wildman, R., Collins, R., Candow, D. G., Kleiner, S. M., Almada, A. L., & Lopez, H. L. (2017). International Society of Sports Nutrition position stand: safety and efficacy of creatine supplementation in exercise, sport, and medicine. Journal of the International Society of Sports Nutrition, 14(1), 18.
Mills, S., Candow, D. G., Forbes, S. C., Neary, J. P., Ormsbee, M. J., & Antonio, J. (2024). Effects of Creatine Supplementation during Resistance Training on Bone Health: A Systematic Review and Meta-analysis. Medicine & Science in Sports & Exercise, 56(1), 118-127.
National Institutes of Health, Office of Dietary Supplements. (2021). Dietary supplements for exercise and athletic performance: Fact sheet for health professionals.
Parada-Flores, B.; et al., (2025). Efectos de la suplementación con creatina monohidratada en la masa muscular y rendimiento físico en adultos jóvenes entrenados: una revisión sistemática. Retos, 62, 958-965.
Rawson, E. S., Newmeyer, M. N., & Srebro, K. J. (2023). Creatine supplementation and cognitive function: An updated review. Nutrition Reviews, 81(8), 912-925.
Valero, A (2026). El arte de cuidar de nuestro cuerpo. Ediciones Agoeiro.
Wang, Z., et al. (2024). Effects of creatine supplementation and resistance training on muscle strength gains in adults <50 years of age: A systematic review and meta-analysis. Nutrients, 16(21), 3665.
[1] A pesar de la comercialización de formas alternativas como la creatina etil éster o la alcalina, las investigaciones actuales demuestran que ninguna de estas variantes supera la eficacia o la seguridad del monohidrato de creatina (o CrM, una vez más, por sus siglas en inglés). Este último se mantiene como el estándar de oro en la suplementación deportiva debido a su biodisponibilidad cercana al 100% y su sólida evidencia en la mejora de la masa muscular y el rendimiento físico (Kreider et al., 2022).
[2] Recurramos a El arte de cuidar de nuestro cuerpo (Valero, 2025) para hablar del ATP: «Durante la práctica de EF el músculo esquelético satisface sus demandas energéticas mediante los sustratos que posee el organismo gracias a la ingestión de los nutrientes presentes en los alimentos, fundamentalmente grasas e hidratos de carbono. Pero la célula muscular no los utiliza directamente; deben primero transformarse en adenosín trifosfato (ATP), por lo que la actividad muscular dependerá del sistema nervioso, de las características bioquímicas y estructurales del músculo y de los diferentes sistemas metabólicos que permiten la reposición y síntesis de ATP, la fuente de energía más rápida e inmediata».
[3] Las células gliales son células del sistema nervioso que no transmiten impulsos como la neuronas, pero las sostienen, las protegen y regulan el entorno químico necesario para su funcionamiento.
BICARBONATO DE SODIO
El bicarbonato de sodio (NaHCO₃) se ha consolidado como un suplemento de categoría A para el Australian Institute of Sport, respaldado por una lógica fisiológica clara: elevar la capacidad amortiguadora extracelular y, con ello, sostener el rendimiento cuando el esfuerzo de alta intensidad empuja al músculo hacia la acumulación rápida de protones[1]. En su posicionamiento, la Sociedad Internacional de Nutrición Deportiva (ISSN, por sus siglas en inglés) indica que dosis de 0,2–0,3 g/kg de peso corporal son eficaces para mejorar el rendimiento en tareas de predominio glucolítico con duraciones aproximadas de 30 segundos a 12 minutos (Grgic et al., 2021). El mecanismo central consiste en favorecer el eflujo de iones de hidrógeno (H⁺) desde el interior de la fibra muscular hacia el espacio extracelular, amortiguando la caída del pH asociada a la acidosis metabólica y retrasando la fatiga en ese rango temporal de esfuerzo. En la práctica, la pauta aguda —administrada 60–180 minutos antes del ejercicio— sigue siendo la más utilizada, pero metaanálisis recientes señalan que los efectos gastrointestinales adversos son frecuentes y pueden neutralizar la ventaja ergogénica; por ello, se han propuesto protocolos de carga crónica y, sobre todo, estrategias de dosis fraccionada como alternativas razonables para preservar el efecto minimizando el malestar (Gough et al., 2019; Senefeld et al., 2019).
Bibliografía:
Gough, L. A., Deb, S. K., Sparks, S. A., & McNaughton, L. R. (2019). The effects of sodium bicarbonate ingestion on cycling performance and time to exhaustion: A systematic review and meta-analysis. Sports Medicine, 49(9), 1431–1442.
Grgic, J., Pedisic, Z., Saunders, B., Artioli, G. G., Schoenfeld, B. J., McKenna, M. J., Bishop, D. J., Kreider, R. B., Stout, J. R., Kalman, D. S., Arent, S. M., VanDusseldorp, T. A., Lopez, H. L., Ziegenfuss, T. N., Burke, L. M., Antonio, J., & Campbell, B. I. (2021). International Society of Sports Nutrition position stand: sodium bicarbonate and exercise performance. Journal of the International Society of Sports Nutrition, 18(1), 61.
Senefeld, J. W., Heden, T. D., Jung, C. P., & Hunter, S. K. (2019). Ergogenic effects of sodium bicarbonate on physical performance: A systematic review and meta-analysis. Sports Medicine, 49(2), 229–251.
[1] Por simplificar, digamos que el bicarbonato ayuda a “neutralizar” parte de la acidez que se acumula fuera de las células musculares durante esfuerzos muy intensos, retrasando la fatiga y permitiendo rendir más tiempo.

BETAALANINA
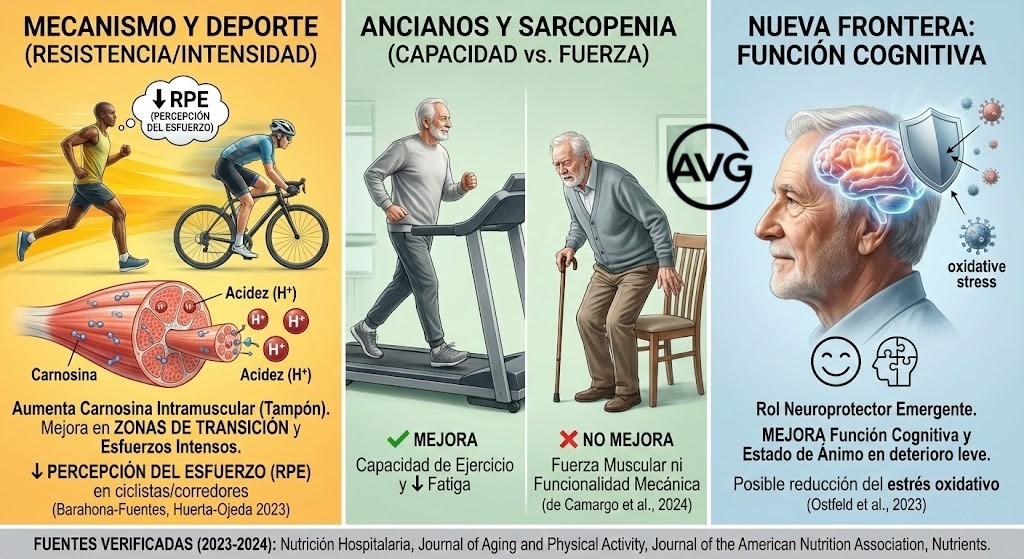
La beta-alanina se ha consolidado como un suplemento de eficacia específica, útil solo cuando el contexto metabólico y la población están bien definidos, y ya no como un ergogénico “universal”. Su mecanismo central —el aumento de la carnosina intramuscular— explica su interés en esfuerzos de alta intensidad, especialmente en zonas de transición aeróbica-anaeróbica. La evidencia reciente, sin embargo, obliga a matizar: en trabajos sobre suplementación aguda en corredores de medio fondo se ha observado una reducción de la percepción subjetiva del esfuerzo (RPE), pero ese efecto no se traduce de forma automática en mejoras uniformes de todos los marcadores fisiológicos si la carga o el protocolo no están bien ajustados (Barahona-Fuentes et al., 2023; Huerta-Ojeda et al., 2022/2023).
Una revisión sistemática con metanálisis en red (Luo et al., 2025) indica que el aumento de la carnosina intramuscular puede mejorar el rendimiento en actividades especialmente condicionadas por una elevada acidosis muscular; en ese marco, la suplementación con beta-alanina resulta relevante porque eleva el contenido de carnosina en el músculo, refuerza su capacidad amortiguadora, atenúa la fatiga y puede mejorar el rendimiento en ejercicios de alta intensidad y corta duración.
En adultos mayores, una revisión sistemática reciente (de Camargo, & Brigatto, 2024) introduce una distinción clínica decisiva: con dosis de 2,4–3,2 g/día, la beta-alanina puede mejorar la capacidad de ejercicio y reducir la fatiga percibida, pero no muestra efectos consistentes sobre la fuerza muscular ni sobre la funcionalidad mecánica (por ejemplo, levantarse de una silla o el equilibrio), por lo que no debería plantearse como tratamiento único frente a la sarcopenia —donde el ejercicio físico adaptado y la alimentación juegan el papel principal e inamovible como estrategia de referencia—. A ello se suma una línea emergente de investigación con interés extra-deportivo: ensayos en mayores sugieren mejoras en función cognitiva y estado de ánimo tras la suplementación, junto con cambios en marcadores relacionados con inflamación y estructura cerebral, lo que abre una vía prometedora que aún exige confirmación clínica más amplia antes de trasladarla a recomendaciones generales (Ostfeld et al., 2023; Ostfeld et al, 2024).
Bibliografía:
Barahona-Fuentes, G., Huerta-Ojeda, A., Galdames-Maliqueo, S., Yeomans-Cabrera, M. M., & Jorquera-Aguilera, C. (2023). Effects of acute beta-alanine supplementation on post-exertion rating of perceived exertion, heart rate, blood lactate, and physical performance on the 6-minute race test in middle-distance runners. Nutrición Hospitalaria, 40(5), 1047–1055.
De Camargo, J. B., Santana, C. C., & Tricoli, V. (2024). Beta-Alanine for Improving Exercise Capacity, Muscle Strength, and Functional Performance of Older Adults: A Systematic Review. Journal of Aging and Physical Activity, 33(4), 399–407.
Huerta-Ojeda, A., Barahona-Fuentes, G., Galdames-Maliqueo, S., & Jorquera-Aguilera, C. (2023). Acute Supplementation with Beta-Alanine Improves Performance in Aerobic-Anaerobic Transition Zones in Endurance Athletes. Journal of the American Nutrition Association, 42(2), 187–194.
Luo, H., Tengku Kamalden, T. F., Zhu, X., Xiang, C., & Nasharuddin, N. A. (2025). Effects of different dietary supplements on athletic performance in soccer players: a systematic review and network meta-analysis. Journal of the International Society of Sports Nutrition, 22(1), 2467890.
Ostfeld, I., Hoffman, J. R., & Stout, J. R. (2023). Role of $\beta$-Alanine Supplementation on Cognitive Function, Mood, and Physical Function in Older Adults: Double-Blind Randomized Controlled Study. Nutrients, 15(4), 923.
Ostfeld, I., Zamir, A., Ben-Zeev, T., Levi, C., Gepner, Y., Peled, D., Barazany, D., Springer, S., & Hoffman, J. R. (2024). β-Alanine supplementation improves fractional anisotropy scores in the hippocampus and amygdala in 60-80-year-old men and women. Experimental Gerontology, 194, 112513.
NITRATOS
La suplementación con nitratos dietéticos (NO₃⁻) se ha consolidado como una de las ayudas ergogénicas con mayor respaldo científico para mejorar la eficiencia metabólica durante el ejercicio, sobre todo por su capacidad para optimizar la vía nitrato-nitrito-óxido nítrico. En términos fisiológicos, este mecanismo puede reducir el coste de oxígeno (VO₂) para una misma carga de trabajo y, por tanto, mejorar la economía del esfuerzo (Jones et al., 2021). Investigaciones recientes también subrayan su efecto sobre la función contráctil, especialmente en fibras musculares de tipo II, donde el óxido nítrico puede favorecer la dinámica del calcio y contribuir a una mayor potencia y velocidad de ejecución (Wylie et al., 2023). En cuanto a la pauta, los protocolos más utilizados sitúan la ingesta en 400–800 mg de nitrato, ya sea mediante una estrategia crónica de 3–7 días o en una dosis aguda única administrada unas 2,5–3 horas antes del esfuerzo. Un detalle a tener en cuenta es evitar colutorios antibacterianos, ya que alteran la microbiota oral responsable de la reducción inicial de nitrato a nitrito y pueden atenuar el efecto ergogénico (Woessner et al., 2021).
Bibliografía:
Gao, C., Gupta, S., Adli, T., & Hou, W. (2021). The effects of dietary nitrate supplementation on graded exercise performance: A systematic review and meta-analysis. Journal of the International Society of Sports Nutrition, 18(1), 7.
Jones, A. M., Thompson, C., Wylie, L. J., & Vanhatalo, A. (2021). Dietary nitrate and exercise performance: New strings to the ergogenic bow. Sports Medicine, 51(Suppl 1), 113–123.
Woessner, M. N., McIlvenna, L. C., Ortiz de Zevallos, J., Neil, C. J., & Allen, J. D. (2021). Dietary nitrate supplementation in cardiovascular health: An ergogenic aid or a therapeutic target? Free Radical Biology and Medicine, 170, 132–147.
Wylie, L. J., Ortiz de Zevallos, J., & Ferguson, S. K. (2023). Nitrate and the fast-twitch muscle fiber: Mechanisms of enhanced power and speed. Current Opinion in Physiology, 31, 100624.

PROTEÍNA
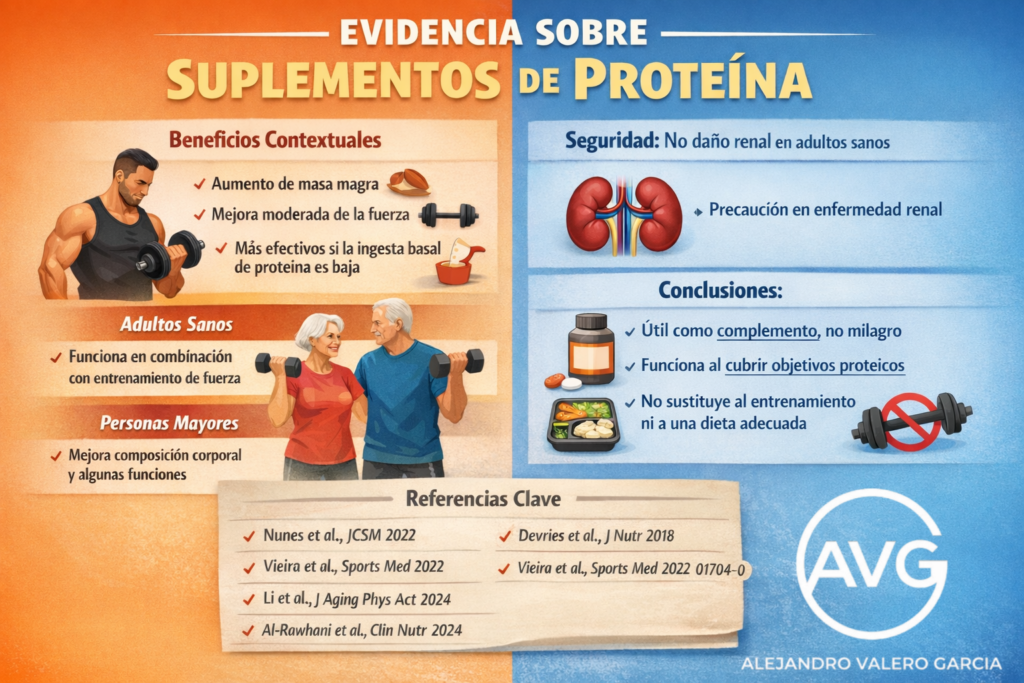
La eficacia de los batidos de proteína se fundamenta en su capacidad para inducir una hiperaminoacidemia rápida y saturar la vía de señalización mTORC1[1], responsable de la síntesis de proteínas miofibrilares. El metaanálisis de referencia de Morton y colaboradores (2018) determinó que la suplementación proteica aumenta significativamente la masa libre de grasa, identificando un punto de saturación en los 1.62 g/kg/día para adultos sanos. La evidencia posterior introduce, no obstante, un matiz decisivo: en situaciones de mayor estrés fisiológico —como restricción energética o cargas elevadas de entrenamiento— las necesidades pueden desplazarse al alza, y en la práctica se contemplan ingestas de hasta 2,2 g/kg/día para preservar mejor la masa magra y el balance nitrogenado (Nunes et al., 2022; Tagawa et al., 2020).
En términos de cinética, la proteína hidrolizada presenta una absorción más rápida que otras formas (utiliza el transportador PEPT1), al aportar una mayor proporción de di- y tripéptidos, lo que puede acelerar la disponibilidad de aminoácidos y favorecer la recuperación en contextos de daño muscular inducido por el ejercicio. Por ello, más que hablar de una proteína “mejor” en abstracto, resulta más preciso distinguir entre objetivos: cubrir la dosis total diaria, optimizar la tolerancia digestiva y, cuando el contexto lo justifica, aprovechar una cinética de absorción más rápida para facilitar la recuperación (Ames et al., 2024; Brown et al., 2022).
Respecto a la función renal, los metaanálisis de Devries y colaboradores (2018) ratifican que el aumento de la Tasa de Filtración Glomerular (GFR) es una respuesta funcional adaptativa y no una nefropatía. El uso de biomarcadores de precisión, como la Cistatina C, confirma la ausencia de daño estructural o estrés glomerular, incluso con ingestas elevadas sostenidas en el tiempo.
En términos de seguridad orgánica, la evidencia disponible en personas sin patología renal o hepática previa no muestra que una ingesta proteica elevada, por sí misma, produzca daño hepático o renal. El hígado dispone de mecanismos eficaces para gestionar el aumento de nitrógeno —principalmente a través del ciclo de la urea— y, en estudios de intervención con sujetos entrenados, incluso ingestas muy altas[2] no han mostrado alteraciones clínicamente relevantes en marcadores de función hepática ni renal dentro del periodo estudiado (Antonio et al., 2016).
En cuanto al riñón, los metaanálisis disponibles señalan que el aumento de la tasa de filtración glomerular (GFR) observado con dietas hiperproteicas en adultos sanos debe interpretarse, en términos generales, como una respuesta funcional adaptativa (hiperfiltración fisiológica) y no como un indicio de nefropatía, especialmente cuando se valoran los cambios pre y posintervención, y no solo los valores finales de forma aislada (Devries et al., 2018). Además, el empleo de biomarcadores como la cistatina C permite afinar la evaluación de la función renal, al no depender exclusivamente de la creatinina sérica; con todo, estos hallazgos no deben extrapolarse a personas con enfermedad renal previa o con riesgo renal establecido.
Finalmente, la evidencia actual no respalda la antigua hipótesis de que una mayor ingesta proteica provoque, por sí misma, descalcificación ósea. Al contrario, una revisión sistemática y metaanálisis de referencia (Shams-White et al., 2017) concluye que una ingesta proteica más alta no perjudica la salud ósea en adultos sanos y puede asociarse a efectos favorables en algunos parámetros, según el contexto dietético y clínico. En este marco, además de la cantidad total diaria, importa la distribución: los consensos de nutrición deportiva suelen situar como referencia práctica tomas de 20–40 g de proteína de alta calidad (aproximadamente 0,25–0,40 g/kg por toma), repartidas a lo largo del día, lo que ayuda a optimizar la síntesis proteica muscular y relativiza una visión rígida de la “ventana anabólica” inmediata (Jäger et al., 2017; Kerksick et al., 2017). Dentro de este marco debemos apelar a la coherencia y señalar que, de nuevo, ni es necesario ni resulta adecuado multiplicar las tomas por encima de lo que exigen los requerimientos reales de cada persona y de cada contexto. En suplementación, como en nutrición, más no equivale automáticamente a mejor; la calidad proteica, la pertinencia de la dosis y su ajuste individual siguen siendo el criterio decisivo.
Respecto al microbioma intestinal, conviene ser prudentes. La digestibilidad de la fuente proteica puede modificar la cantidad de sustrato nitrogenado que llega al colon, pero la respuesta intestinal depende del patrón dietético global, de la dosis total y de la microbiota basal de cada persona. Por ello, no sería riguroso formular una conclusión general sobre un efecto “optimizador” de los suplementos aislados sobre la salud del microbioma sin una revisión específica de esa literatura. No hemos abordado todos los suplementos útiles ni la extensión que merecen y, en casos como la creatina o la suplementación proteica, un desarrollo completo puede resultar excesivamente técnico para parte de los lectores —e, incluso, aburrirles, como es comprensible—. Por eso, dedicaremos una entrada complementaria a la suplementación de proteínas, con más detalle.
Bibliografía:
Ames, C. T., Brown, M. A., & Phillips, S. M. (2024). Protein hydrolysates versus intact proteins: An updated review of postprandial muscle protein synthesis and recovery. Journal of Applied Physiology, 136(2), 442–455.
Antonio, J., Ellerbroek, A., Silver, T., Vargas, L., & Peacock, C. (2016). The effects of a high protein diet (4.4 g/kg/d) on body composition in resistance-trained individuals. Journal of the International Society of Sports Nutrition, 13(1), 19.
Brown, M. A., Stevenson, E. J., & Howatson, G. (2022). Whey protein hydrolysate supplements and recovery from exercise-induced muscle damage: A systematic review. Applied Physiology, Nutrition, and Metabolism, 47(3), 231–241.
Devries, M. C., et al. (2018). Changes in kidney function do not differ between healthy adults consuming higher-protein diets and a control or lower-protein diet: A systematic review and meta-analysis. Clinical Journal of the American Society of Nephrology, 13(11), 1623–1632.
Jäger, R., Kerksick, C. M., Campbell, B. I., Cribb, P. J., Wells, S. D., Skwiat, T. M., Purpura, M., Ziegenfuss, T. N., Ferrando, A. A., Arent, S. M., Smith-Ryan, A. E., Stout, J. R., Arciero, P. J., Ormsbee, M. J., Taylor, L. W., Wilborn, C. D., Kalman, D. S., Kreider, R. B., Willoughby, D. S., … Antonio, J. (2017). International society of sports nutrition position stand: Protein and exercise. Journal of the International Society of Sports Nutrition, 14, 20.
Kerksick, C. M., Arent, S., Schoenfeld, B. J., Stout, J. R., Campbell, B., Wilborn, C. D., Taylor, L., Kalman, D., Smith-Ryan, A. E., Kreider, R. B., Willoughby, D., Arciero, P. J., VanDusseldorp, T. A., Ormsbee, M. J., Wildman, R., Greenwood, M., Ziegenfuss, T. N., Aragon, A. A., & Antonio, J. (2017). International society of sports nutrition position stand: Nutrient timing. Journal of the International Society of Sports Nutrition, 14, 33.
Morton, R. W., et al. (2018). A systematic review, meta-analysis and meta-regression of the effect of protein supplementation on resistance training-induced gains in muscle mass and strength in healthy adults. British Journal of Sports Medicine, 52(6), 376–384.
Nunes, J. P., et al. (2022). Protein supplementation and resistance training: An overview of systematic reviews and meta-analyses. Nutrition Reviews, 80(4), 784–801.
Shams-White, M. M., et al. (2017). Dietary protein and bone health: a systematic review and meta-analysis from the National Osteoporosis Foundation. The American Journal of Clinical Nutrition, 105(6), 1528–1543.
Tagawa, R., et al. (2020). Dose–response relationship between protein intake and muscle mass increase: A systematic review and meta-analysis of randomized controlled trials. Nutrients, 12(8), 2365.
[1] Una vez más, recurrimos a un extracto de El arte de cuidar de nuestro cuerpo (Valero, 2025) para explicar que: «La vía mTOR se activa en respuesta a ejercicios de fuerza y ayuda a controlar varias funciones celulares, puesto que regula tanto la síntesis de proteínas como la biogénesis de los ribosomas (es decir, el proceso mediante el cual se producen estos orgánulos celulares en los que tiene lugar la síntesis de proteínas). La estimulación de esta vía conduce a la hipertrofia muscular y esta se produce mediante ejercicios con cargas mecánicas altas (como ocurre con el ejercicio de fuerza), aunque no debemos olvidar que sin el adecuado aporte nutricional y descanso, no va a producirse con eficiencia la síntesis de proteínas; el trabajo con cargas como el crecimiento muscular depende de la biogénesis ribosómica». En este contexto, mTORC1 es el complejo específicamente más implicado en la regulación de la síntesis proteica muscular
[2] Dosis de hasta 4.4 g/kg/día no alteran las transaminasas hepáticas, aunque apuntamos que tales dosis ni son necesarias, ni convenientes.
CONCLUSIONES
La revisión de estos suplementos permite extraer una conclusión de fondo que conviene preservar frente al ruido habitual que forma el batiburrillo compuesto por el mercado, usuarios, detractores e iluminados. Ante esto, ceñirnos a la etimología de la palabra y contemplarlos como un suplemento, no como un sustituto. La utilidad de una ayuda ergogénica nunca depende solo de su popularidad, sino de la relación entre mecanismo, dosis, contexto fisiológico y objetivo concreto, todo ello supeditado a la calidad de la evidencia científica que posea cada suplemento.
En ese cruce se decide todo. Un mismo compuesto puede ser valioso en un escenario —por ejemplo, cuando interesa amortiguar la fatiga, sostener el rendimiento en esfuerzos determinados o preservar masa muscular en situaciones de desuso— y, al mismo tiempo, resultar marginal o innecesario en otro. Por eso, una lectura madura de la suplementación exige criterio de aplicación, ajuste individual y expectativas bien medidas, alejada de atajos y cimentada en criterio.
Si bien son pocos los suplementos que gozan de un respaldo científico que avale sus resultados, con demasiada frecuencia se exageran beneficios parciales hasta convertirlos, por simple extrapolación, en promesas casi taumatúrgicas. En ese juego —hecho de semántica, ambigüedad y márgenes legales— se presenta al posible comprador una eficacia desmedida, como si tuviera entre las manos el auténtico bálsamo de Fierabrás. De ahí el propósito de estas páginas: reunir algunos suplementos que sí pueden resultar útiles en contextos concretos y, al mismo tiempo, reivindicar el conocimiento para que guíe nuestras decisiones.
Entender esa diferencia evita errores frecuentes, desde el uso redundante hasta expectativas desproporcionadas, y permite integrar la suplementación, si es que es necesaria, donde de verdad tiene sentido: como herramienta auxiliar de una estrategia mayor, subordinada al entrenamiento, la alimentación, el descanso y la situación clínica individual. Comprender esa arquitectura evita usos redundantes y expectativas desproporcionadas, y permite integrar la suplementación donde realmente aporta valor: como herramienta auxiliar dentro de una estrategia más amplia, vinculada al entrenamiento, la alimentación, el descanso y la situación clínica individual.
Para concluir, añadiremos que utilizar suplementación es una decisión que debe ser motivada por una carencia, adaptando los protocolos de uso tanto a las demandas específicas de una metodología de ejercicio físico concreta o de una modalidad deportiva, como a las características individuales de cada sujeto; la excelencia nutricional debería aspirar a que el suplemento sea solo un actor de reparto, convocado únicamente cuando la especificidad del contexto así lo exija. Debemos hacer un buen uso de la información que recibamos y procurar una base de conocimiento necesario para dar material a nuestro raciocinio a la hora de procesar dicha información, porque, tal y como podemos leer en El arte de cuidar la mente (Valero, 2025), «en ocasiones, la información que nos llega cuando solo nos fijamos en lo agradable del discurso e interlocutor, es aquella de quien utiliza un tono y expresión más acorde acerca de lo que entenderíamos como correcto, no de quien mejores argumentos traiga en cuanto a la evidencia disponible y mayor conocimiento posea de la cuestión a tratar»[1].
[1] Valero, A (2025). El arte de cuidar la mente. McGraw-Hill – AULAMAGNA.

Cómo citar esta publicación:
Valero, A. (2026). Una revisión de la literatura científica sobre los suplementos nutricionales con mayor evidencia. Alejandro Valero García. Disponible en: https://alejandrovalerogarcia.com/una-revision-de-la-literatura-cientifica-sobre-los-suplementos-nutricionales-con-mayor-evidencia/

